Alt om osmium

Osmium - et sjældent metal, tilhører platingruppen. Det blev opdaget i England som et resultat af eksperimenter med platins reaktion. Navnet osmium er givet på græsk og betyder i oversættelse "lugt". Hvordan er dette ædle metal? Hvad er dens funktioner, og hvad er dens brug?

Historie
Opdagelsen af dette grundstof skete ved et uheld i 1803 af de engelske kemikere Smithson Tennant og William H. Wollastan. Som et resultat af eksperimenter med platins reaktion på en blanding af syrer (svovlsyre og salpetersyre) udviklede det resulterende bundfald en ubehagelig aroma, der minder om stanken af klor og rådden radise. Lignende eksperimenter blev udført af Colle-Descoti, Antoine de Fourcoy og Vauquelin i Frankrig. Som et resultat af deres forskning fandt de også et ukendt stof i det uopløselige sediment fra platin.



Det dengang ukendte stof hed chick, men briternes eksperimenter viste, at der er tale om to lignende stoffer - iridium og osmium.
Opdagelsen af disse kemiske elementer blev præsenteret for Royal Society i London ved Tennants skriftlige meddelelse dateret 21. juni 1804. I det periodiske system af kemiske elementer i Mendeleev er metallet placeret under ordensnummeret 76. Metallet forekommer ikke i sin rene form af nuggets, derfor præsenteres dets kemiske formel i opløst form.


Grundstoffet udvindes fra sekundære råmaterialer som et resultat af dets adskillelse fra iridium-, platin-, platin-palladiummalme eller kobber- og nikkelmalme. Den årlige produktion af hele elementet i verden overstiger ikke størrelsen på 1 ton.


Fødselssted
Verdens største forekomster er værd at bemærke sådanne zoner som Uralbjergene og Sibirien i Rusland, nordstat Alaska og den vestlige stat Californien i Amerika, Canada i Nordamerika, Colombia i Sydamerika og nogle sydafrikanske lande, Australien, Ø Tasmanien... I øjeblikket overvejes en betydelig osmiumforekomst Bushwell Complex i Sydafrika, det meste af stoffet udvindes der. Når man tager i betragtning, at de største forekomster af metallet er i Sydafrika, er verdenspriserne for dette sjældne jordarters metal ret høje. Kasakhstan betragtes som den eneste store eksportør af osmium-187 i verden. Selvom Kina har platinmalmreserver, har det ikke betydelige mængder osmium.


Stoffet opbevares i pulverform og da det ikke smelter i form af krystaller, er det ikke muligt at sætte et stempel på det på grund af dets fysiske egenskaber. Til fremstilling af ingots af dette metal anvendes elektronstråle- eller lysbueopvarmning fra et pulver; opvarmning i en digel bruges også.


Ejendomme
Osmium ligner et sølvfarvet blåligt metal. Det er et af de tætteste grundstoffer, dens massefylde er 22.600 kg per kubikmeter, men samtidig er stoffet ret skrøbeligt, knækker let og smuldrer. Den har en høj vægtfylde og er i stand til at skinne selv ved ret høje temperaturpåvirkninger. På grund af dets parametre og betydelige smeltetemperatur er det svært at bearbejde det. I naturen eksisterer det i form af syv isotoper, hvoraf seks anses for at være stabile, disse er osmium-184, osmium-187, osmium-188, osmium-189, osmium-190 og osmium-192. Radioaktive metalisotoper med massetal fra 162 til 197 blev opnået i laboratoriet, og nogle nukleare isomerer blev også fremstillet kunstigt.
Osmium påvirker i kraft af dets egenskaber alle levende organismer negativt.

Næsten alle forbindelser med dette metal forårsager skade på indre organer, visuelle og auditive lidelser. Ved forgiftning med osmiumdampe kan der opstå irreversible forstyrrelser i kroppen og død. Forskere udførte forsøg på dyr, hvis resultater var den hurtige udvikling af anæmi, manglen på normal lungefunktion. Det blev konkluderet, at dette er et hurtigt udviklende ødem. Osmiumtetroxid, som bruges i medicin, er et meget ætsende stof. Har den grimmeste lugt i verden. I tilfælde af forgiftning lider huden, den skifter farve til grøn eller sort, ofte ledsaget af sår og revner, som vil tage meget lang tid at hele.

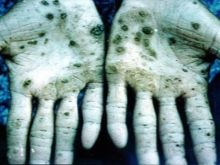

Ansatte i produktionsfaciliteter er i den højeste risiko; i henhold til alle sikkerhedsstandarder arbejder de kun i åndedrætsværn og specielt tøj. Alle beholdere indeholdende osmiumoxid er forseglet og opbevaret i overensstemmelse med reglerne. For at opnå mineralerne fra nevyanskite omdannes platin til en opløsning ved hjælp af aqua regia. Derefter udsættes det resulterende bundfald for zink i en 8-dobbelt mængde - en sådan legering omdannes relativt let til en pulverform, som derefter smeltes sammen med bariumperoxid. Det næste trin er behandlingen af den resulterende masse med aqua regia, destillation gennem apparatet til adskillelse af osmiumtetroxid.

Ved at virke på stoffet med en alkaliopløsning opnås salt. Saltopløsningen påvirkes hyposulfit, hvorved metallet ved hjælp af ammoniumchlorid udfældes allerede i form af Fremys salt. Bundfaldet vaskes, filtreres og kalcineres. Resultatet af alle disse handlinger er svampet osmium. Efterfølgende renses det med syrer, reduceres i en elektrisk ovn under en brintstrøm og afkøles. Så få osmiumprøver op til 99,9 %.


Kemisk
Egenskaberne af dette element, fra et kemisynspunkt, er fantastiske. De mest grundlæggende af dem er følgende.
- Osmium reagerer slet ikke med baser og syrer. Danner vandopløselige osmater i reaktion med alkaliske smelter. Interaktion med en blanding af salpetersyre og saltsyre giver en ekstrem langsom reaktion.
- Meget giftig, selv i mikroskopiske doser. Særligt giftigt er osmiumoxid, som frigives fra platin.
- Det er umuligt at bestemme metallets kogepunkt, da det er særligt ildfast.
- Metallet i pulveret indgår let i en opvarmningsreaktion med sådanne stoffer: ren oxygen, halogener, svovlsyre eller salpetersyre.
- I forskellige forbindelser opnås oxidtal fra -2 til +8. De mest almindelige er +2, +3, +4 og +8.
- I stand til at danne klyngeforbindelser.
- De vigtigste mineraler er relateret til faste opløsninger og er repræsenteret af legeringer af iridium med osmium - de er sysertskite og nevyanskite. Desuden har syserskite et andet navn - iridisk osmium og nevyanskite - osmøst iridium.

Fysisk
Massefylde osmium er cirka 22,61 gram per kubikcentimeter. Krystaller har en smuk sølvskinnende glans, med forskellige nuancer fra grå til blå. I ingots vises en mørkeblå farve, i pulveret er den violet. Alt metal har en sølvskinnende glans. Toksiciteten af elementet forhindrer dets anvendelse i smykkeindustrien. De vigtigste fysiske egenskaber er som følger.
- Smeltepunktet for dette element er ret højt, smeltning er mulig ved temperaturer over 3000 grader Celsius.
- Metal har ingen magnetiske egenskaber.
- Fantastisk fasthed. Legeringer med tilsætning af dette metal opnår øget slidstyrke, holdbarhed, korrosionsbestandighed og modstand mod mekanisk belastning.
- Kogepunktet er 5012 ºC.
- Mohs hårdhed er 7.
- Vickers hårdhed er 3-4 GPa.

Ansøgninger
På grund af de betydelige omkostninger ved selve elementet bruges dette metal sjældent i masseindustriel produktion. Osmium bruges hovedsageligt i den kemiske industri, hvor det bruges som katalysator. Osmiumtetroxid bruges i nogle lægemidler. I laboratorieanalyser bruges det til farvning af levende væv, sikrer bevarelsen af cellestrukturen.
I rumfartsindustrien bruges osmium i det elektroniske udstyr til udstyr til luftfart og raketteknologi, såvel som i fremstillingen Atom våben. På grund af manglen på magnetiske egenskaber, metallet bruges til fremstilling af mærkevareure som Rolex. Legeret osmium med platin bruges når oprettelse af kirurgiske implantater Er pacemakere eller lungeventiler.
Derudover bruges osmium til mikroskopi og til at skabe højpræcisionsinstrumenter.



Interessante fakta
- Under et tryk på omkring 770 GPa i osmium interagerer elektroner i indre orbitaler, strukturen af stoffet forbliver uændret.
- Osmium i klipperne indeholder en halv procent af den samlede masse af malmforekomster.
- På grund af den høje tæthed metallets udseende og faktiske vægt varierer meget. Så en 0,5 liters plastflaske fyldt med dette metalpulver vil være tungere end en 10 liters spand fyldt med vand.
- Dette metal er i de fem mest kostbar.
- Prisen for en tredobbelt ounce osmium er en forretningshemmelighed, i åbne kilder kan du finde en omtrentlig pris for 1 gram af et stof.
- På grund af osmiums ildfasthed noteret i historien om den elektriske lampe. Videnskabsmanden K. Auer von Welsbach fra Tyskland fremsatte et forslag om at erstatte kulstoftråden i en pære med en osmiumglødetråd. Pærerne viste sig at være 3 gange mindre energikrævende, og belysningen er blevet markant forbedret. Sandt nok blev det snart erstattet af det mere almindelige tantal, som igen blev erstattet af wolfram.
- En lignende situation skete med det sjældne metal i ammoniakproduktionen. Den i øjeblikket anvendte metode til ammoniaksyntese, udviklet i 1908 af kemikeren Fritz Haber fra Tyskland, er umulig uden brug af katalysatorer.Oprindeligt viste de katalysatorer, der blev brugt på det tidspunkt, deres egenskaber kun i nærværelse af betydelige temperaturforhold og havde ikke høj effektivitet, så søgningen efter en erstatning var meget presserende. Forskere fra laboratoriet på den højere tekniske skole i Karlsruhe fremsatte et forslag om at bruge fint forstøvet osmium som et katalytisk element. Testresultaterne bekræftede, at denne idé er umagen værd, den katalytiske temperatur er faldet med mere end 100 ºC, og frigivelsen af ammoniak er steget betydeligt. Sandt nok nægtede de osmium i fremtiden, men han hjalp med at løse et så vigtigt problem.

Osmium og andre sjældne og unikke metaller spiller væsentlig rolle i forskellige brancher... Selv med al dens toksicitet redder den liv og sundhed for mennesker.
For mere information om osmium, se følgende video.








